grupos funcionales orgánicos
En química orgánica, el grupo funcional es un conjunto de átomos unidos a una molécula de cadena abierta, suelen ser representados genéricamente por R (radicales alquílicos), mientras que los aromáticos, o derivados del benceno, son representados por Ar (radicales arílicos).
 |
Las series homólogas y grupos funcionales listados a continuación son los más comunes.1 En las tablas, los símbolos R, R', o similares, pueden referirse a una cadena hidrocarbonada, a un átomo de hidrógeno, o incluso a cualquier conjunto de átomos.
vídeo de los grupos funcionales
grupos funcionales orgánicos
| Grupo funcional | Serie homóloga | Fórmula | Estructura | Prefijo | Sufijo | Ejemplo |
|---|---|---|---|---|---|---|
| Grupo hidroxilo | Alcohol | R-OH | hidroxi- | -ol | ||
| Grupo alcoxi (o ariloxi) | Éter | R-O-R' | -oxi- | R-il R'-il éter | ||
| Grupo carbonilo | Aldehído | R-C(=O)H |  | formil- | -al
-carbaldehído2
|  |
| Cetona | R-C(=O)-R' |  | oxo- | -ona |  | |
| Grupo carboxilo | Ácido carboxílico | R-COOH |  | carboxi- | Ácido -ico | 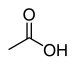 |
| Grupo acilo | Éster | R-COO-R' |  | -iloxicarbonil- | R-ato de R'-ilo |
Cada grupo funcional determina las propiedades químicas de las sustancias que los poseen; es decir, determina su función química.
Entonces, se llama función química a las propiedades comunes que caracterizan a un grupo de sustancias que tienen estructura semejante; es decir, que poseen un determinado grupo funcional.
1.- Óxidos: (Ácidos, Básicos, Neutros, Peróxidos y Su peróxidos).
2.- Hidróxidos.
3.- Ácidos: (Hidróxidos y Oxácidos).
4.- Sales: (Haloideas y Oxisales (Neutras, Ácidas, Básicas y Dobles)).
5.- Hidruros: Metálicos y no Metálicos
Éteres
Se llaman éteres los compuestos formados por dos radicales unidos entre sí, mediante enlaces sencillos, a un átomo de oxígeno (O). El grupo funcional es R – O – R (alcoxi). Los radicales ( R ) que se unen al oxígeno pueden ser iguales o diferentes.
Para nombrarlos, se antepone la palabra éter al nombre de los radicales; si éstos son iguales se menciona el radical anteponiendo el prefijo “di” y agregando la terminación “ico”; si los radicales son diferentes se nombra en primer lugar el de cadena más corta más el nombre del otro al que se le añade la misma terminación “ico”.
Algunos ejemplos de éteres son:
CH3 – CH2 – O – CH2 – CH3 éter dimetílico (los dos radicales son iguales)
CH3 - O – CH2 - CH3 éter metiletílico (radicales distintos)
CH3 – CH2 – O – CH2 – CH2 - CH3 éter propílico
|



No hay comentarios:
Publicar un comentario